《临床和转化医学》最新发布|标准化是干细胞疗法持续快速健康发展的关键
来源: 发布日期:2024-07-05 浏览次数:1092次
随着医疗技术的进步和生活质量的提高,替换或再生受损组织正在成为现实,作为再生医学重要组成部分,干细胞疗法为众多疑难杂症患者带来了希望,其独有的特性可以修复人体受损细胞和组织。
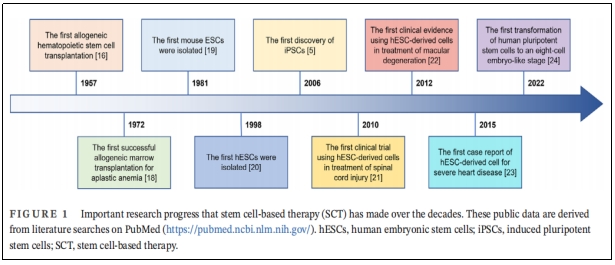
世界上第一例有记录的同种异体造血干细胞(HSC)移植治疗白血病是在1957年完成,由于骨髓移植在当时是未知的,参与该项研究的6名患者最终全部死亡,只有2名患者表现出短暂植入证据。
在接下来2年,研究人员发现健康同卵双胞胎的骨髓可以用于治疗白血病,此后经过数十年快速发展,该领域取得了许多重大进展。如ESC和iPSC的发现,以及它们在不同疾病中的应用,这不仅提高了研究人员和患者对干细胞治疗(SCT)疾病的信心,也推动了干细胞市场快速发展(图1)。
尽管SCT具有广阔应用前景,但目前还尚未实现大规模临床应用。当事情没有按预期进行时,通常意味着标准化的缺失。SCT从小规模、定制实验向常规临床实践的转变需要标准化协助,标准化不仅可以帮助SCT安全、有效发展,还可以防止其过早商业化。
SCT临床应用现状
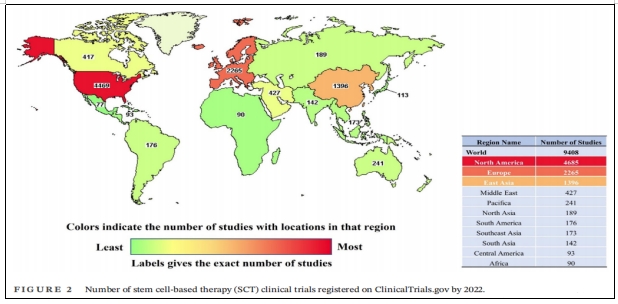
为了加快SCT临床应用,在前期动物实验安全性数据基础上,世界各国开展了广泛的SCT临床试验,截至2022年12月,已超过9400项干细胞相关试验在临床试验网站注册(www.clinicaltrials.gov),这些数据反映出SCT对世界各地研究人员的强烈吸引力(图2)。
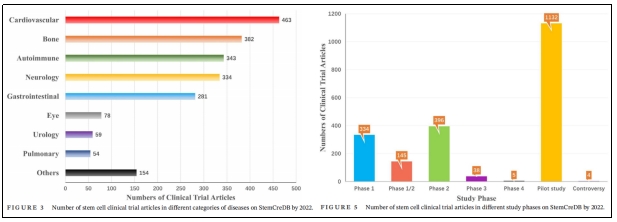
根据干细胞临床研究数据库(DB)统计,目前SCT临床试验涉及心血管、骨骼、神经、免疫、胃肠、肺、泌尿、眼科等。其中SCT临床试验文章大多集中在前五类,心血管系统疾病研究数量最多(图3)。此外,大部分试验仍处于探索性研究阶段,III期及以上临床试验数量相对较少(图5),SCT要实现大规模临床应用还有一定距离。
SCT市场发展现状
临床试验增加,带动了SCT市场规模显著增长。根据Global Market Insight发布的2021年SCT市场报告,2020年全球SCT市场规模达到89亿美元,其中北美市场份额为41.5%,这可能受益于当地政府大力支持。该报告还预测,2021年~2027年SCT市场规模将以超过10.6%/年的增长率持续增长。
SCT相关标准制定现状
SCT无论在疾病治疗还是市场规模上都取得了令人瞩目成就,但SCT包含一个完整而复杂的过程,涉及细胞采集、培养、运输、检测等多个环节,任何一个环节操作不规范都可能影响SCT效果。
目前全球许多国家、地区和国际组织都制定了相应的SCT标准,这将有力推动SCT进一步发展,只有标准化才能根据合理的科学原理,确保对干细胞产品、生产设施、治疗效果和市场趋势进行顺利、高效评估。
ISO的SCT相关标准
ISO是一个国际标准制定组织,由167个不同国家的标准机构组成,它制定的标准得到了世界各地专家认可。其中参与SCT相关标准制定的技术委员会(TC)主要是ISO/TC 276 Biotechnology,ISO/TC 276已发布26项标准,其中12项与细胞治疗相关。
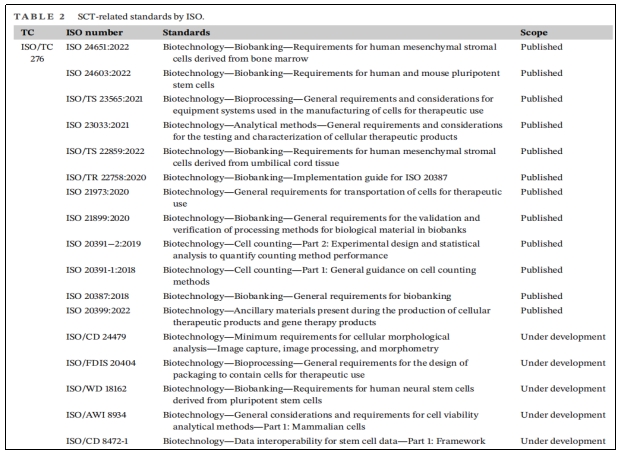
与细胞治疗相关ISO标准不仅包括已发布标准,还包括正在制定标准,ISO标准是世界各地专家智慧结晶,它们可以有效提高SCT标准化水平,对整个行业标准化和人类健康具有重要意义(表2)。
国际组织制定的SCT相关标准
为了及时有效地补充和更新相关SCT标准,出现了一些国际组织,以协助SCT标准制定。例如血液和生物治疗促进协会(AABB)是一个国际性非营利组织,它为采购、加工、储存或分销细胞治疗产品的机构制定标准并对其进行认证。
细胞治疗认证基金会(FACT)是由国际细胞和基因治疗学会(ISCT)和美国移植和细胞治疗学会(ASTCT)共同创立的非营利组织,为细胞治疗高质量发展制定标准,在FACT制定的标准中,与SCT相关标准主要包括造血细胞治疗标准、脐带血库标准和通用标准。
FACT标准内容全面,不仅涵盖细胞制剂临床应用前的收集、加工、储存、运输、管理等各个阶段,还包含临床应用的整个过程。ISCT不仅参与了FACT标准制定,还独立制定了SCT相关标准,包括最小标准和MSCs免疫学表征。
国际干细胞研究协会(ISSCR)作为从事干细胞研究重要国际专业组织,对SCT设定了很高标准。自2006年以来,ISSCR已经发布了4项关于干细胞研究和临床转化指南,促进了干细胞领域的科学探索和伦理考虑。
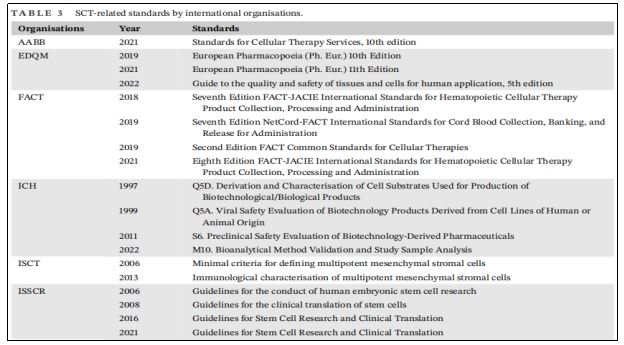
在欧洲,欧盟委员会通过建立欧洲药品和保健质量理事会(EDQM)制定与细胞移植相关指导和标准,EDQM出版的欧洲药典包含多项细胞治疗质量控制标准。EDQM也发布了相应指南,最新指南不仅包含适用于所有参与组织和细胞捐献、采购、检测、加工、保存、储存和分配的组织机构和组织的一般要求,还包含针对各种组织和细胞的具体指南和要求,但欧洲制定SCT相关标准并不能完全适用于其他国家或地区。
为了实现更广泛地区药物开发和监管标准统一,欧洲、日本和美国组织的代表讨论并成立了国际协调理事会(ICH),所有ICH指南主题分为四类:质量指南、安全指南、功效指南和多学科指南,它们将确保安全、有效和高质量药物开发和注册(表3)。
国家组织制定的SCT相关标准
世界各国都在以单一标准追求全球自由贸易,但在当前形势下实现这一目标难度很大。一方面,现有国际标准很难覆盖SCT全过程。另一方面,不同国家具体情况差异很大,同一国际标准不一定适用于所有国家。对此各个国家标准机构在采用ISO标准基础上,会根据实际需要对国际标准进行调整和补充,制定国家标准(表4)。
英国标准协会(BSI)成立于1901年,是世界上第一个国家标准机构,BSI公开发布了多项SCT相关规范文件,为了帮助提高细胞产品、服务和系统的质量和安全性。德国标准化研究所( DIN)是德国和全球标准化独立平台,DIN发布的标准规定了生物库中储存生物材料样品容器一般要求。法国标准化协会(AFNOR)在2016年发布了一项标准,该标准不是细胞培养手册,是提供了允许生产用于动物健康病毒学或血清学诊断的细胞培养物要求和建议。
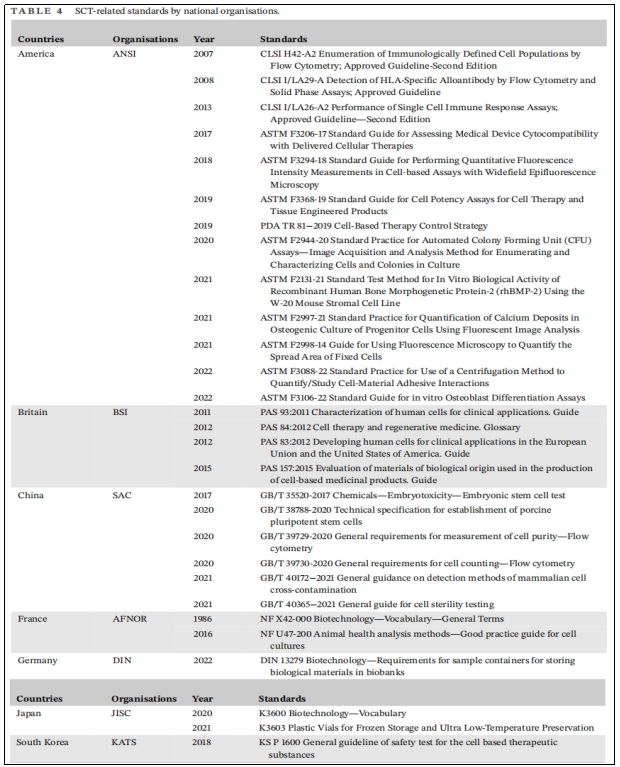
美国国家标准(ANS)是由美国国家标准协会(ANSI)通过认可标准开发组织(SDO)的程序并批准其文件过程来制定的,其制定SCT相关标准的SDO主要包括美国测试与材料协会(ASTM)、临床和实验室标准协会(CLSI)和肠外药物协会(PDA)。
中国公布的国家标准内容比较丰富,这些标准包括特定细胞(如胚胎干细胞)的规范要求,以及细胞纯度、计数、交叉污染和无菌测试。日本工业标准委员会(JISC)发布了生物技术词汇和细胞冷冻保存容器的标准。韩国技术标准局(KATS)也发布了基于细胞治疗物质的安全性测试一般指南。
此外,还有许多国家也制定了与SCT相关国家标准,如瑞典、澳大利亚、新西兰等。除国家标准外,每个国家还可能有团体标准、行业标准和地方标准,这些标准将在特定领域补充国家标准,在世界各国努力下,SCT标准化工作逐渐趋于完善。
总 结:经过几十年的发展,SCT在临床研究和市场规模上取得了令人瞩目的成就,它强大的再生和修复能力,使许多不治之症有了逆转可能。SCT产业健康快速发展离不开相应标准所起到的积极引导作用,这些标准有效地协调了不同国家和地区之间的药物开发和监管,提高了干细胞相关产品应用效率。
随着干细胞相关研究不断深入,SCT标准化体系构建也在不断完善,标准化和质量控制可以确保SCT的安全性和有效性。相信不久的将来,SCT将真正实现从实验室研究向大规模临床实践转变。
参考资料:
Zhang J, Suo M, Wang J,et al. Standardisation is the key to the sustained, rapid and healthy development of stem cell-based therapy. Clin Transl Med. 2024;14:e1646.Doi:10.1002/ctm2.1646.
















